一、主要业务
百奥泰生物制药股份有限公司致力于开发新一代创新药和生物类似药,用于治疗肿瘤、自身免疫性疾病、心血管疾病以及其它危及人类生命或健康的重大疾病。
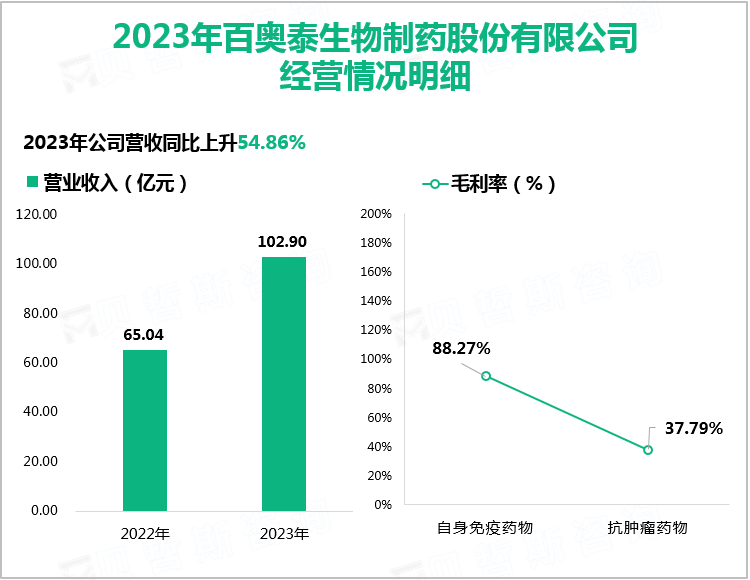
2023年百奥泰生物制药股份有限公司经营情况明细
二、公司所处的行业地位分析及其变化情况
公司自创立以来就建立了具有领先技术水平的研发平台和具有成本优势的生产技术平台,并通过不断优化升级,突破新药研发和生产中的技术断点和瓶颈,持续开发并商业化具有自主知识产权、安全、有效、患者可负担的创新药物,以实现我国自主研发和生产的生物药进入海内外市场、惠及全球患者、树立领先生物制药国际品牌的目标。
在生物类似药领域,目前已有三款产品成功上市:格乐立®是公司自主研发的阿达木单抗生物类似药,自2020年1月起开始进行格乐立®的商业销售。
截至当前,格乐立®的销售网点已覆盖中国除港澳台地区的其他省、直辖市、自治区,与超过1000家处方医院及超过1200家药店达成合作,并已在中国除港澳台地区的其他省、直辖市、自治区成功挂网。其BAT1706(贝伐珠单抗)在报告期内获得美国FDA批准上市,美国商品名为Avzivi®,Avzivi®是第二个由中国药企研发且获得美国FDA上市批准的生物类似药产品,公司已于全球多区域及地区开展了BAT1706(贝伐珠单抗)的商业化进程。
BAT1706(贝伐珠单抗)已于2021年11月获国家药监局批准上市,商品名为普贝希®,公司已与百济神州有限公司签订合作协议,由百济神州有限公司将进行普贝希®在中国市场(包括中国大陆、中国香港特别行政区、中国澳门特别行政区、中国台湾地区)的开发和商业化。BAT1806(托珠单抗)于2023年1月获得国家药监局的上市批准,中国商品名为施瑞立®,施瑞立®是国内获批的首个托珠单抗生物类似药,亦是全球首个托珠单抗生物类似药。
BAT1806(托珠单抗)于2023年9月获得美国FDA的上市批准,美国商品名为TOFIDENCE,TOFIDENCE是公司第一个获得美国FDA上市批准的产品,是FDA批准的首个托珠单抗生物类似药,亦是第一个由中国本土药企自主研发、生产且获得美国FDA上市批准的单克隆抗体药物。此外,BAT1806(托珠单抗)也已向欧洲EMA递交上市许可申请。
|
|
营业收入(亿元) |
|
医药制造 |
7.05 |
数据源自:贝哲斯根据公开资料整理

我们提供更专业明智的市场报告,让您的商务决策锦上添花。


400-166-9286
181-6370-6525

贝哲斯客服

